SCI论文解读(26):肿瘤细胞通过纳米管结构获取免疫细胞线粒体并实现免疫逃逸
发布单位: 广东省医学会医学科研实验室建设与管理学分会 / 阅读:2779 次 / 2022/1/5 8:18:27
 王珊,广州医科大学附属第二医院副研究员,华南理工大学微生物学博士,美国芝加哥大学博士后,目前就职于广东省过敏反应与免疫重点实验室。主要从事食物过敏发病机制与防治研究,包括儿童食物过敏发病与免疫耐受的机制、肠道菌群与代谢调控食物过敏的机制研究。主持国家自然科学基金、广东省科技厅项目。2017年入选广州医科大学高水平大学学术骨干,2019年入选广州市高层次人才青年后备人才。现为广东省医学会医学科研实验室建设与管理学分会实验技术学组副组长。
王珊,广州医科大学附属第二医院副研究员,华南理工大学微生物学博士,美国芝加哥大学博士后,目前就职于广东省过敏反应与免疫重点实验室。主要从事食物过敏发病机制与防治研究,包括儿童食物过敏发病与免疫耐受的机制、肠道菌群与代谢调控食物过敏的机制研究。主持国家自然科学基金、广东省科技厅项目。2017年入选广州医科大学高水平大学学术骨干,2019年入选广州市高层次人才青年后备人才。现为广东省医学会医学科研实验室建设与管理学分会实验技术学组副组长。

1. 引言
肿瘤细胞有多种实现免疫逃逸的方式,从而保证自身的存活发展。深入研究免疫逃逸的具体机制,才能为肿瘤的免疫治疗提供方向。2021年11月18日,美国哈佛医学院的研究人员在《Nature Nanotechnology》期刊上发表了题为:Intercellular nanotubes mediate mitochondrial trafficking between cancer and immune cells 的研究论文,该团队发现肿瘤细胞一种独特的免疫逃逸方式:肿瘤细胞可以与免疫细胞之间形成一种纳米级的管道,而肿瘤细胞则会通过这些微管来“劫持”免疫细胞的线粒体,此消彼长下肿瘤细胞便完成了免疫逃逸。
2. 结果展示
1)肿瘤细胞与免疫细胞间形成纳米管
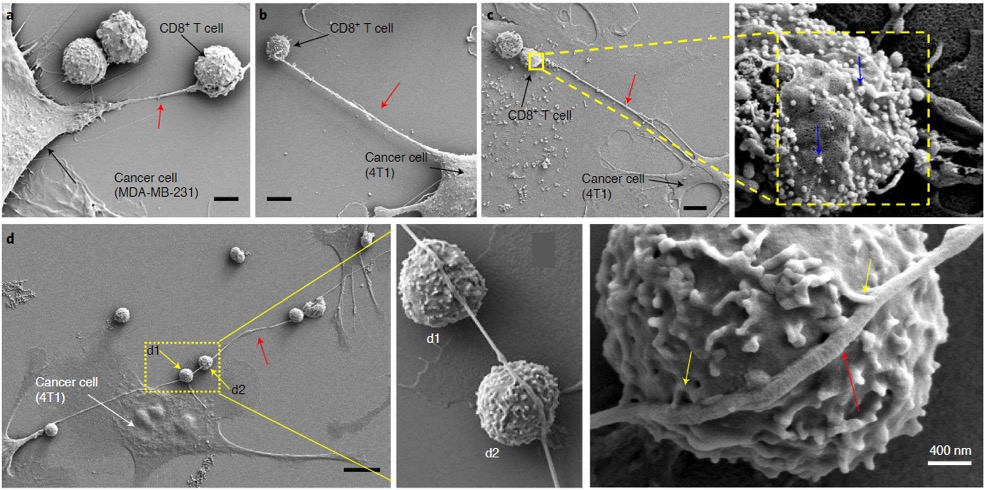
研究初期作者通过扫描电镜发现肿瘤细胞与免疫细胞间会形成一种纳米管,这种纳米管通常长11-30μm,直径100-1000nm,从肿瘤细胞发出,连接沿途的多个免疫细胞。值得注意的是虽然此次研究中发现平均每个癌细胞会伸出一根纳米管,但是作者提到,考虑到样品制作过程中的损耗,许多较为脆弱的纳米管实际上并未被检测到,因此纳米管的实际数量很可能更多。
2)纳米管介导肿瘤细胞与免疫细胞之间的线粒体转移
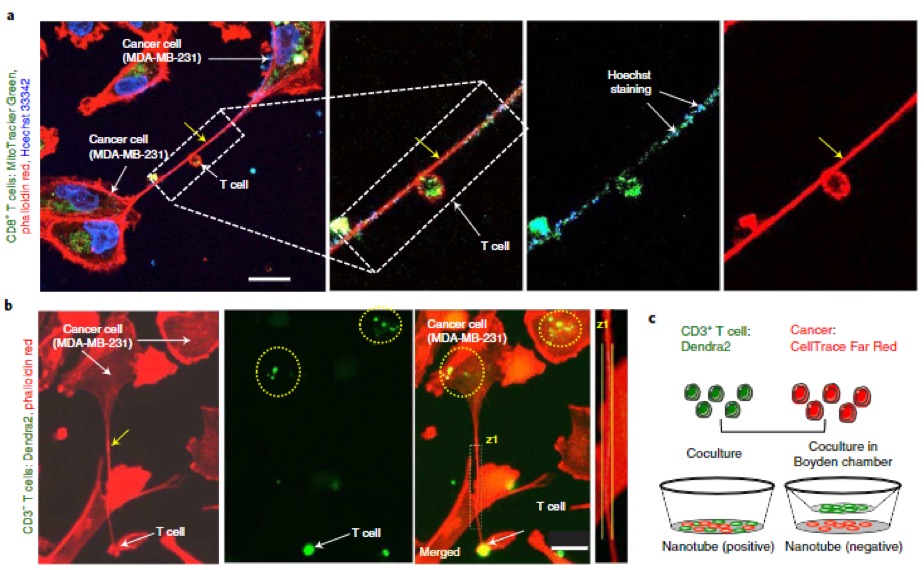
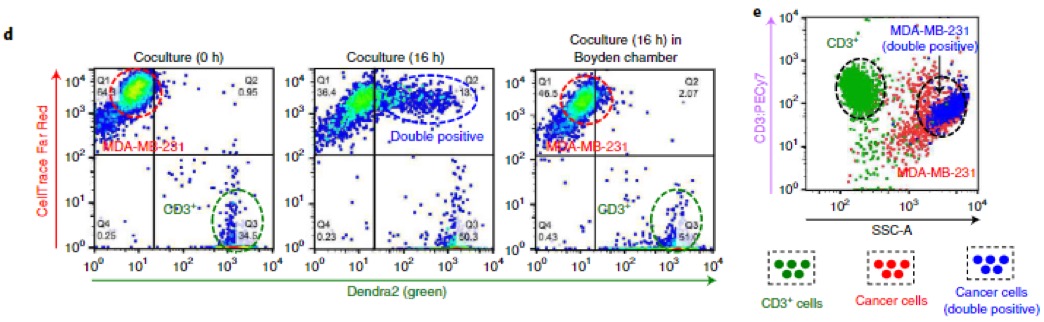
既往的研究发现类似的纳米管结构往往介导对机体有害的反应,例如在T细胞间传递HIV病毒,在神经细胞之间传递朊病毒。因此作者认为肿瘤细胞极有可能是通过这种纳米管来实现免疫逃逸。考虑到线粒体的重要性,作者决定检测纳米管是否促进线粒体的转移。结果显示,确实纳米管会介导线粒体的转移。为了更好地说明确实是纳米管介导的线粒体转移,而不是染料泄露等原因造成的结果误判,作者设置了免疫细胞单独培养16h后,取培养基培养癌细胞,免疫细胞与癌细胞共培养及通过Transwell将癌细胞和免疫细胞隔离开培养三组。结果显示取培养基培养癌细胞及Transwell组并未出现线粒体着色,而共培养组癌细胞出现明显线粒体转移的迹象。
3)线粒体转移影响了双方细胞的呼吸功能
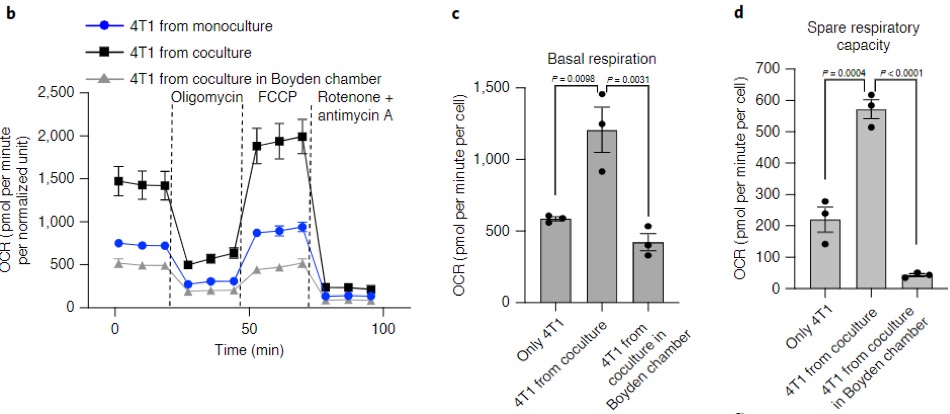
作者进行了代谢分析来进一步研究线粒体转移带来的影响。结果显示共培养组癌细胞出现明显的呼吸功能上调,而免疫细胞的呼吸功能明显减弱。
4)肿瘤细胞的外囊复合体介导了细胞间纳米管形成
此前研究表明,纳米管的形成与外囊复合体有关。作者通过敲除肿瘤细胞外囊复合体形成的关键基因,验证了肿瘤细胞主动“窃取”免疫细胞的线粒体,并且外囊复合体在纳米管形成乃至线粒体转移中起到重要作用。
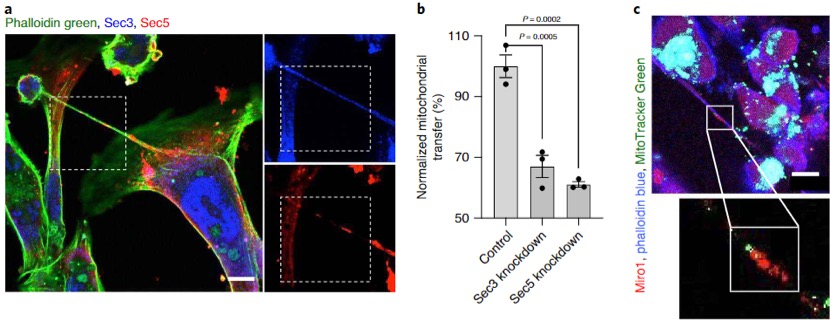
5)线粒体转移抑制免疫细胞活性与数量
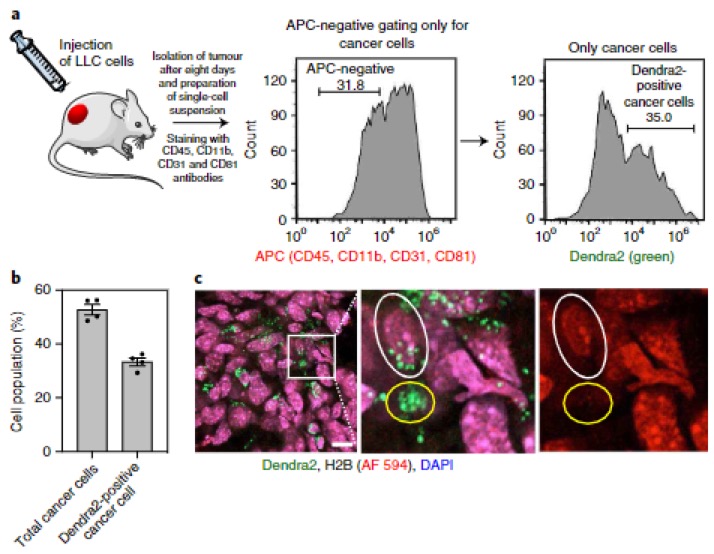
作者通过实验发现在肿瘤发展的早期,肿瘤细胞数量还未明显增多时,由于线粒体的缺失,免疫细胞出现了明显的减少,这为临床的早期检测提供非常重要的提示。小鼠体内实验发现,35%的肺癌细胞都会出现线粒体转移,而当抑制纳米管形成后肿瘤大小明显变小,免疫细胞数量明显增多。
3. 研究思路
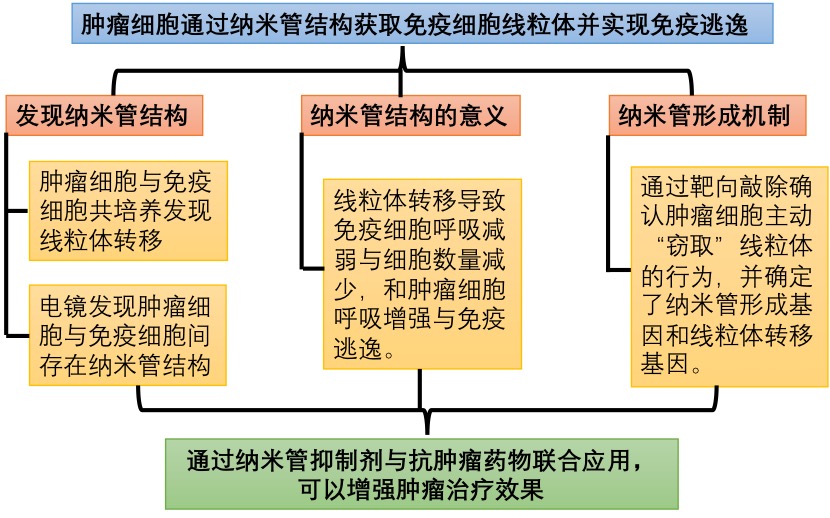
4. 总结
本次研究首次发现,癌细胞可以通过线粒体转移的方式增加自身的呼吸能力,降低免疫细胞的呼吸能力,从而实现免疫逃逸。同时作者发现针对纳米管形成的药物L-778123联合现有免疫制剂(PD-1)时,能够明显抑制肿瘤的生长,为临床治疗提供了新的思路及理论基础。除此以外,本次研究侧重于描述发现了免疫细胞线粒体转运至癌细胞这一现象,而例如为何癌细胞会向某些细胞定向形成纳米管,线粒体为何是从免疫细胞定向迁移至癌细胞等诸多问题还需要深入探究,这些结果极有可能催生新一代的免疫疗法。
原文链接:https://www.nature.com/articles/s41565-021-01000-4 (Nature Nanotechnology,IF=39.213)


