SCI论文解读(38):Gasdermin D通过与阿霉素直接结合和线粒体损伤的变化介导阿霉素诱导的心肌细胞焦亡和心脏毒性
发布单位: 广东省医学会医学科研实验室建设与管理学分会 / 阅读:4494 次 / 2023/7/3 15:15:55
 蔡轶,广州医科大学药学院,副研究员,硕士生导师,2012年毕业于中山大学获得博士学位。曾在美国加州大学洛杉矶分校和新加坡国立大学进行访问学者研究工作。主要研究方向为心血管药理学和肿瘤药理学,目前以第一作者或通讯作者身份发表SCI论文20余篇。
蔡轶,广州医科大学药学院,副研究员,硕士生导师,2012年毕业于中山大学获得博士学位。曾在美国加州大学洛杉矶分校和新加坡国立大学进行访问学者研究工作。主要研究方向为心血管药理学和肿瘤药理学,目前以第一作者或通讯作者身份发表SCI论文20余篇。

1. 引言
阿霉素(Dox)是一种广泛使用的蒽环类抗肿瘤药物,可引起严重的心脏毒性。心肌细胞死亡和炎症参与Dox诱导的心脏毒性(DIC)的病理生理学过程。Gasdermin D (GSDMD)被称为焦亡的“关键执行者”,焦亡是一种促炎性程序性细胞死亡。我们旨在研究GSDMD对DIC的影响,并系统揭示其潜在机制。我们的研究结果表明,Dox通过siRNA或过表达质粒技术以GSDMD依赖的方式诱导心肌细胞焦亡。然后,我们通过CRISPR/Cas9系统产生GSDMD全基因敲除小鼠,发现GSDMD缺陷减少了Dox诱导的心肌病。Dox诱导炎性caspases的激活,进而间接介导GSDMD-N的生成。通过分子动力学模拟和无细胞系统,我们证实Dox直接与GSDMD结合并促进GSDMD- N介导的焦亡。此外,GSDMD还通过Bnip3和线粒体穿孔介导Dox诱导的心肌细胞线粒体损伤。这些发现为Dox参与的GSDMD如何协调不良心脏毒性的机制提供了新的见解,并突出强调了GSDMD作为DIC潜在靶点的前景。
2. 结果展示
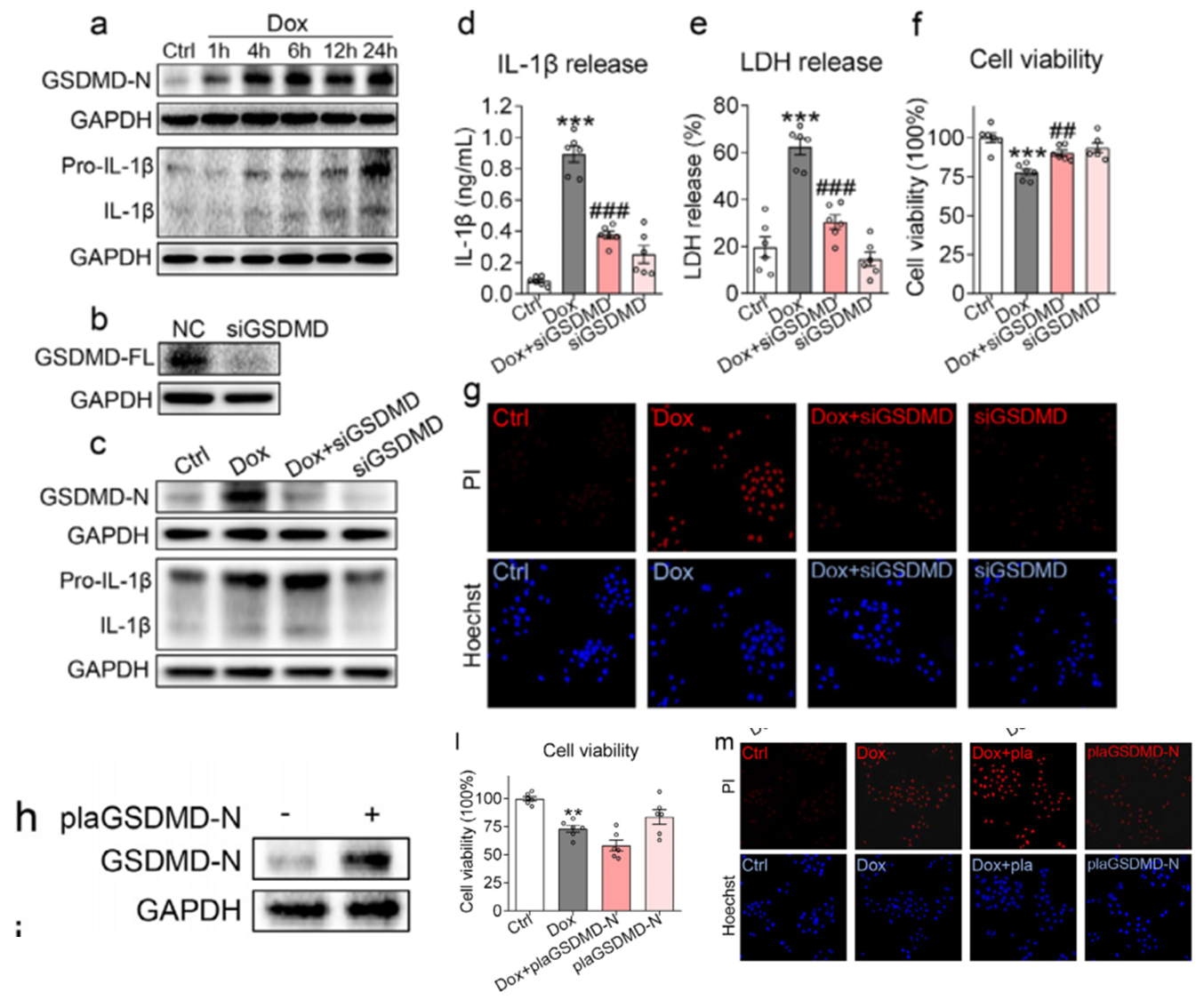
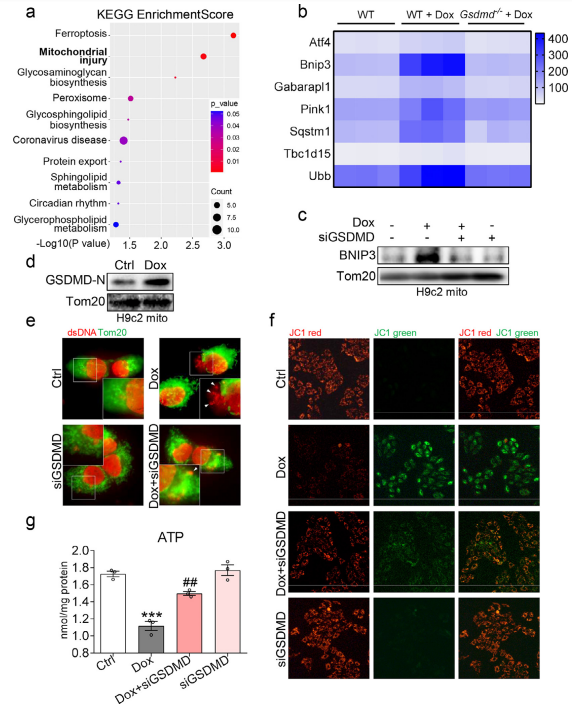
1)Dox通过GSDMD依赖性方式诱导心肌细胞焦亡。本研究选择1 mM Dox进行体外实验,通过Western blot检测pro-IL-1b和关键焦亡蛋白GSDMD-N水平。为了确定GSDMD参与Dox诱导的心肌细胞焦亡,本研究在Dox暴露前沉默了GSDMD的表达,进行转染特异性siRNA的原代心肌细胞蛋白水平检测和CCK8实验。进一步还进行了原代心肌细胞转染GSDMD-N表达质粒实验。为确定GSDMD蛋白在Dox诱导心肌细胞焦亡发挥的关键作用,本研究还进行细胞活力测定和PI染色实验。
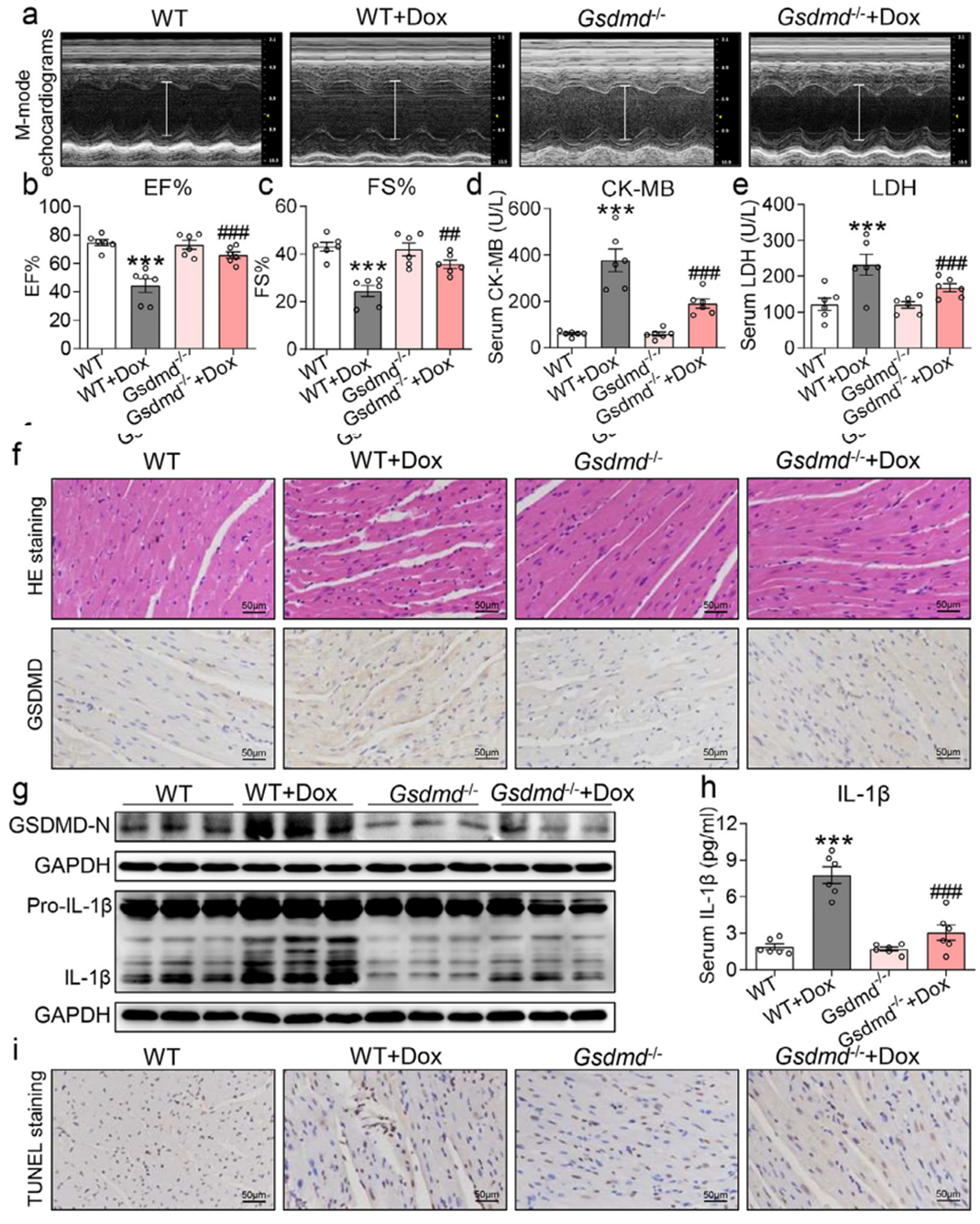
2)为研究体内GSDMD缺乏对Dox诱导的心肌焦亡和心脏毒性的作用。本研究采用GSDMD全局敲除小鼠,采用无创经胸超声心动图测定心脏功能,并采用H&E染色心脏组织来测量心肌细胞结构异常。进一步为研究GSDMD依赖性焦亡在体内的作用,采用免疫组织化学和Western blot检测相关蛋白的表达,结果表明GSDMD缺乏可减少Dox诱导的心肌焦亡和体内心脏毒性。
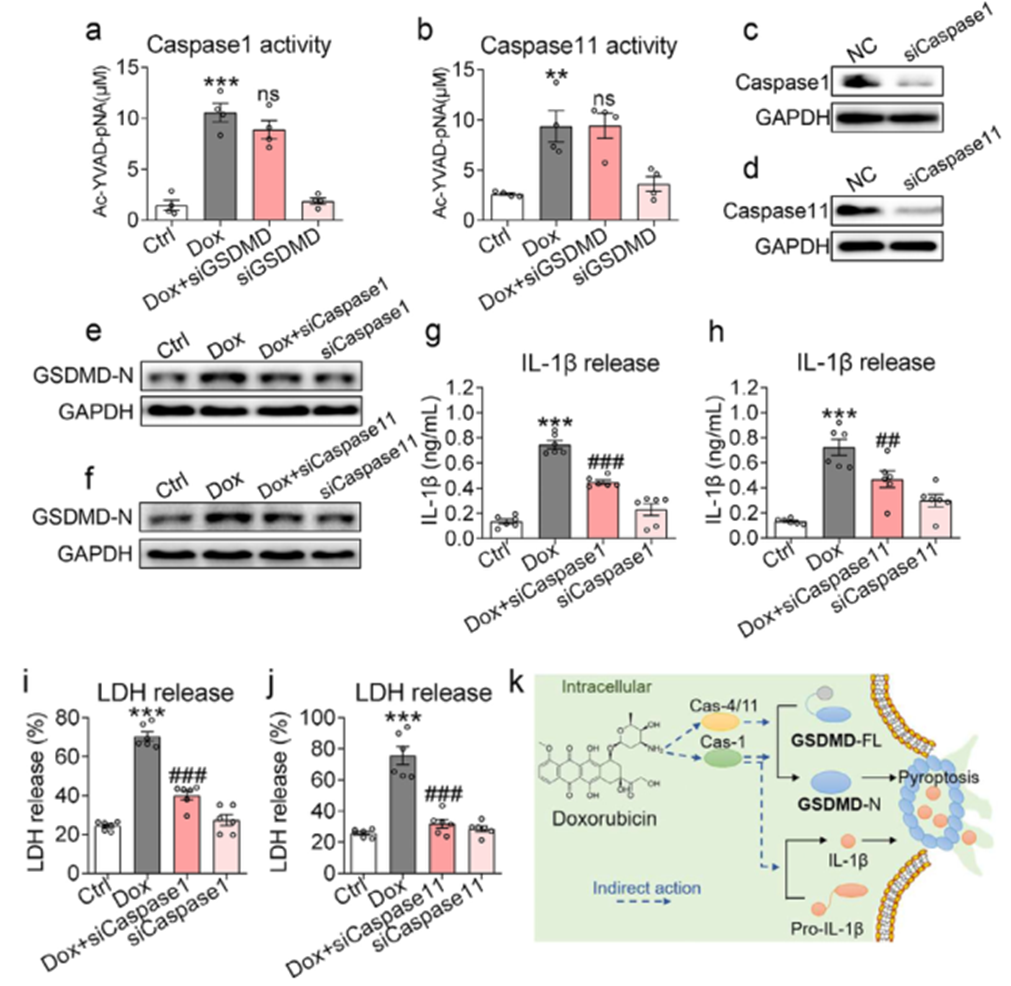
3)炎性半胱天冬酶介导Dox刺激心肌细胞产生GSDMD-N和焦亡。本研究分析了炎性caspases的活性,发现GSDMD在焦亡中的功能位于炎性半天冬酶的下游。进一步验证炎性Caspase在Dox刺激的心肌细胞中切割GSDMD,原代心肌细胞通过siRNA沉默Caspase1和Caspase11。结果证实沉默Caspase1消除了Dox诱导的心肌细胞的pyroptosis,如IL-1b分泌、LDH释放和细胞活力。这些结果证明Caspase1和Caspase11在Dox刺激的心肌细胞中均介导GSDMD- n的生成和pyroptosis,GSDMD是Caspase1/11的共同底物。
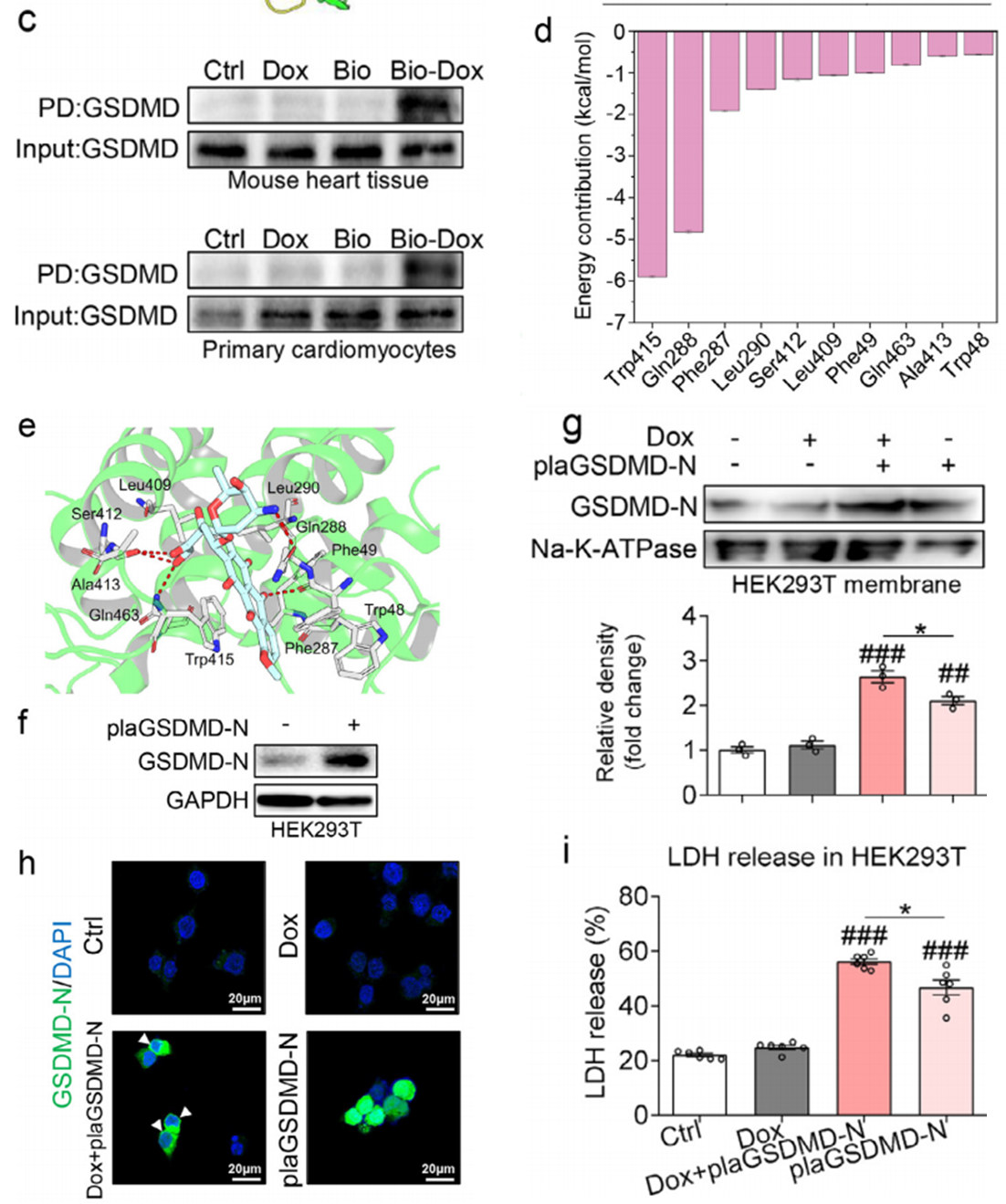
4)Dox直接结合GSDMD促进GSDMD- N介导的焦亡。为研究Dox独立于炎性caspases激活GSDMD的其他潜在机制,本文通过分子对接和MD模拟,预测hGSDMD与Dox可能的相互作用,并分析了GSDMD的所有主原子和Dox的重原子的RMSDs,以确定所研究的体系达到平衡。为证实该结果,本研究利用生物分子层干涉测量法(BLI)来确定Dox-GSDMD的直接相互作用,同时使用表面等离子体共振(SPR)证实ITC数据。为确定Dox是否在心脏组织裂解液和原代心肌细胞中与GSDMD结合,本研究进行了下拉实验。进一步研究Dox结合GSDMD的潜在结构机制发现,Dox可能通过结合残基Phe49和Leu290干扰GSDMD的自抑制作用,促进其膜低聚。最后,为确定Dox与GSDMD联合使用是否会影响GSDMD- N的功能,本研究以低表达Caspase1和Caspase4/ 11的HEK293T为工具细胞,用表达GSDMDN的质粒转染HEK293T。
5)线粒体损伤是DIC过程中GSDMD的下游致病机制。为了更好地描述GSDMD调控DIC的下游致病机制,本研究对WT和GSDMD的心脏组织进行了RNA-seq分析实验。为了确认过度活跃的线粒体损伤通路的潜在作用,我们测量了心脏组织中线粒体损伤相关基因的mRNA水平,发现Bnip3参与了Dox诱导的心肌细胞焦亡。此外,本研究通过测量线粒体靶向抗氧化剂MitoTEMPO的作用来测试GSDMD-调控的线粒体损伤是否介导了pyroptosis,表明GSDMD通过Bnip3和线粒体穿孔介导Dox诱导的线粒体损伤,线粒体损伤是GSDMD的下游致病机制,与质膜穿孔无关。
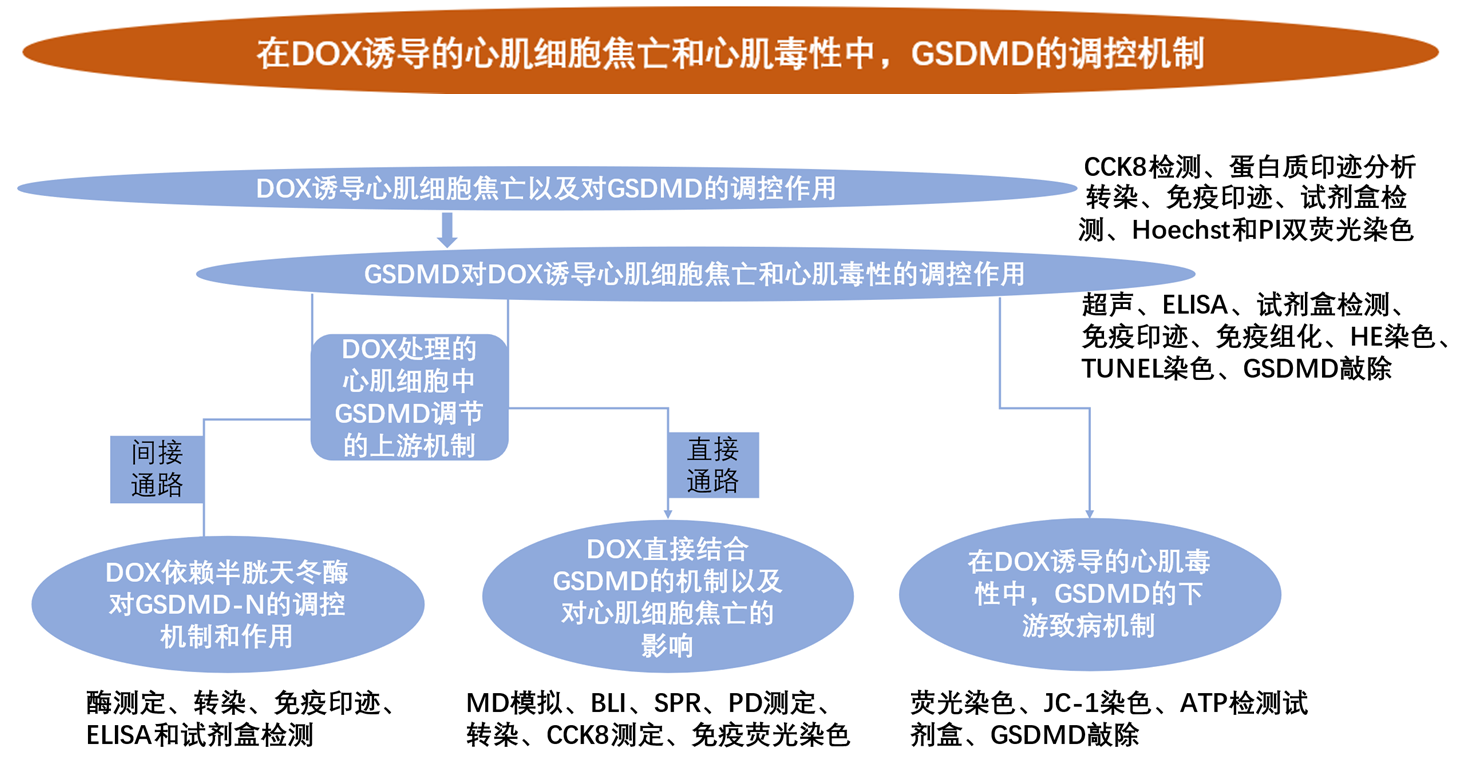
3.研究思路
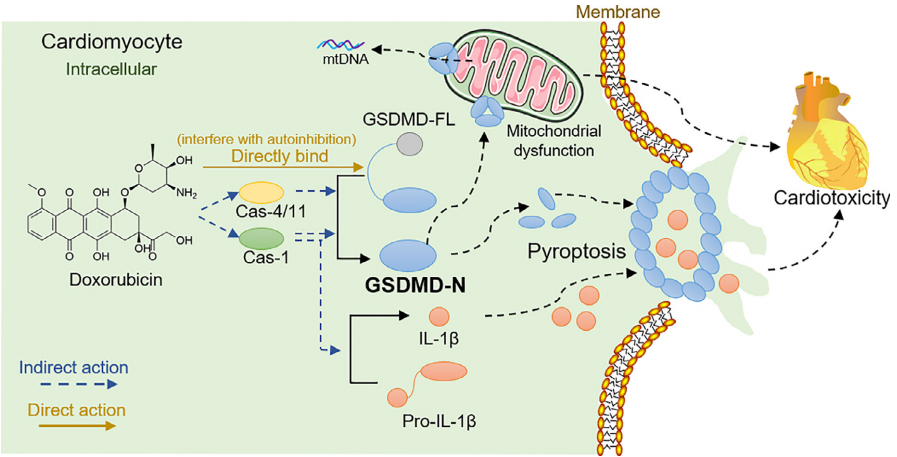
4. 总结
以下关键发现支持Dox参与的GSDMD相关致病机制作为DIC背后的中心驱动力:(1)Dox以GSDMD依赖的方式诱导心肌细胞焦亡,GSDMD缺乏减少了Dox诱导的小鼠心肌病;(2)Dox诱导炎性胱天蛋白酶的激活,随后间接介导GSDMD-N的生成和焦亡;(3)Dox直接与GSDMD结合并促进GSDMD-N介导的焦亡;(4)GSDMD还通过Bnip3和线粒体穿孔介导Dox诱导的线粒体损伤。这些发现为GSDMD如何协调不良心脏毒性的机制提供了见解,并突出了GSDMD作为DIC潜在靶点的前景。
原文链接:https://doi.org/10.1016/j.trsl.2022.05.001(IF=6.542)


